Molti protozoi vivono nel corpo umano. Molti di loro sono patogeni. La nostra storia parla di dieci di loro, la maggior parte. La recensione si basa su pubblicazioni sia storiche che attuali.
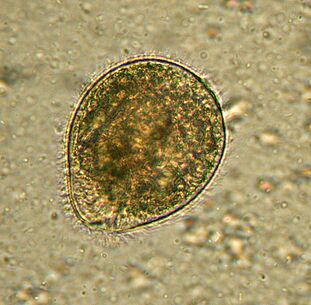
più grande. BalantidiumBalantidium coli
Il più grande protozoo è un parassita umano e l'unico ciliato in questa azienda. Le sue dimensioni variano da 30 a 150 micrometri di lunghezza e da 25 a 120 micrometri di larghezza. Per fare un confronto: la lunghezza del plasmodium della malaria nello stadio più grande è di circa 15 micrometri ed è molte volte più corta del balantidium delle cellule intestinali sotto cui vivono gli infusori. Un elefante in un negozio di porcellane.
Distribuitoovunque ci siano maiali: i portatori principali. Di solito vive nella sottomucosa dell'intestino crasso, sebbene si trovi anche nell'epitelio polmonare nell'uomo. Si nutre di batteriB. coli, particelle di cibo e frammenti dell'epitelio ospite. Negli animali l'infezione è asintomatica. Le persone possono sviluppare diarrea grave con secrezione sanguinolenta e viscida (balantidiasi) e talvolta si formano ulcere nelle pareti del colon. È raro morire di balantidosi, ma provoca stanchezza cronica.
Le persone vengono infettate da acqua sporca o cibi che contengono cisti. Il tasso di infezione nell'uomo non supera l'1%, mentre i suini possono essere infettati in tutto il mondo.
Trattato con antibioticinon sono stati ancora pubblicati rapporti di farmacoresistenza di questo ciliato.
Scoperto dallo scienziato svedese Malstem nel 1857. La balantidosi oggi è associata alle aree tropicali e subtropicali, alla povertà e alla scarsa igiene.
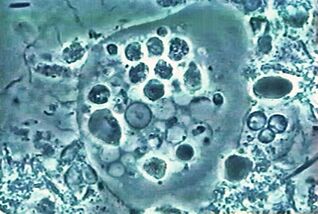
Il primo. Ameba oraleEntamoeba gingivalis
La prima ameba parassita trovata negli esseri umani. La descrizione dell'ameba fu pubblicata nella più antica rivista scientifica nel 1849. Amoeba trovata nella placca, da cui il nome dal latino gingiva - gomme.
Vivenella bocca di quasi tutti coloro che hanno dolori ai denti o alle gengive, abita nelle tasche gengivali e nella placca. Si nutre di cellule epiteliali, leucociti, microbi e, nel caso degli eritrociti. È raro nelle persone con una cavità orale sana.
Questo piccolo protozoo con una dimensione da 10 a 35 µm non penetra nell'ambiente e non forma cisti. Viene trasmesso a un altro ospite attraverso baci, piatti sporchi o cibo contaminato. E. gingivalisè considerato un parassita puramente umano, ma a volte si trova in gatti, cani, cavalli e scimmie in cattività.
All'inizio del XX secolo,E. gingivalisè stato descritto come causa di parodontite perché è sempre presente nelle cellule dei denti infiammate. Tuttavia, la patogenicità non è stata dimostrata.
I farmaciche influenzano questa ameba sono sconosciuti.
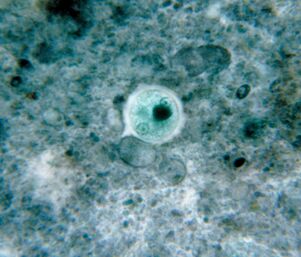
Il più utilizzato. Dissenteria amebaEntamoeba histolytica
Questo parassita intestinale con il sangue invade i tessuti del fegato, polmoni, reni, cervello, cuore, milza e genitali. Mangia ciò che ottiene: particelle di cibo, batteri, eritrociti, leucociti e cellule epiteliali.
Distribuito ovunque, specialmente ai tropici. Di solito, le persone vengono infettate ingerendo una ciste.
Nei paesi temperati l'ameba rimane nel lume intestinale e l'infezione è asintomatica. Il processo patologico inizia spesso nei tropici e subtropicali:E. histolyticaattacca le pareti. Le ragioni del passaggio alla forma patogena non sono ancora chiare, ma sono già stati descritti diversi meccanismi molecolari alla base. Quindi è chiaro che l'ameba secerne sostanze lisanti, sfonda il muco e uccide le cellule. Apparentemente l'ameba può distruggere la cellula ospite in due modi: innescando l'apoptosi o semplicemente masticando pezzi. Il primo metodo è stato a lungo considerato l'unico. A proposito, il meccanismo del suicidio cellulare a una velocità record - in pochi minuti - non è stato identificato. Il secondo metodo è stato descritto solo di recente, gli autori lo hanno chiamato trogocitosi dal greco "tre" - rosicchiare. È interessante notare che l'ameba che morde le cellule lascia la preda non appena muore. Altri possono fagocitare completamente le cellule morte. Si ritiene che le cellule che mordono e divorano differiscano nel modello di espressione genica.
Adesso la capacità dell'ameba di invadere il flusso sanguigno, il fegato e altri organi è collegata alla troocitosi.
L'amebiasi è una malattia mortale. Ogni anno circa 100. 000 persone muoiono a causa di un'infezione daE. histolytica.
La dissenteria ha un gemello non patogeno,E. dispar, quindi la microscopia non è sufficiente per diagnosticare la malattia.
Per la guarigione, ilE. histolytica mobile deve essere distruttoe cisti.
DescrisseE. histolyticae ne determinò la natura patogena in un paziente con diarrea nel 1875. Il nome latino per l'ameba fu dato nel 1903 dallo zoologo tedesco Fritz Schaudin.Histolyticasignifica distruggere i tessuti. Nel 1906 lo scienziato morì per un ascesso intestinale amebico.
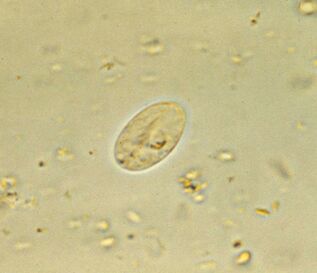
Il più comune. Lamblie intestinaleGiardia lamblia (G. intestinalis)
Giardia, il parassita intestinale più comune, è onnipresente. Il 3-7% delle persone nei paesi sviluppati e il 20-30% nei paesi in via di sviluppo sono infetti. Sono circa 300 milioni di persone.
I parassiti vivononel duodeno e nei dotti biliari dell'ospite, dove si librano, lavorano con i flagelli e poi si attaccano all'epitelio con l'aiuto di un disco appiccicoso sul lato inferiore della cellula. Per 1 cm2l'epitelio aderisce a un milione di lamblia. Danneggiano i villi, che influenzano l'assorbimento dei nutrienti e provocano infiammazioni delle mucose e diarrea. Quando la malattia colpisce le vie biliari, è associata all'ittero.
La giardiasi è una malattia delle mani sporche, dell'acqua e del cibo. Il ciclo vitale di un protozoo è semplice: c'è una forma attiva nell'intestino e all'uscita ci sono cisti stabili con materia fecale. Per essere infettati, è sufficiente ingoiare una dozzina di cisti, che nell'intestino tornano in una forma attiva.
Il segreto principaledell'ubiquità della lamblia nella variabilità delle proteine di superficie. Il corpo umano combatte la lamblia con gli anticorpi ed è in linea di principio in grado di sviluppare l'immunità. Ma le persone che vivono nella stessa zona e bevono la stessa acqua continuano a essere infettate dalla prole dei loro stessi parassiti. Perché? Perché durante il passaggio dalla fase attiva alla cisti e viceversa, la lamblia cambia le proteine contro le quali vengono prodotti gli anticorpi - proteine di superficie specifiche per variante. Ci sono circa 190 varianti di queste proteine nel genoma, ma solo una è sempre presente sulla superficie di un singolo parassita, la traduzione del resto è interrotta dal meccanismo dell'interferenza dell'RNA. E il cambiamento avviene all'incirca ogni dieci generazioni.
Vienetrattato con un agente antiprotozoico con attività antibatterica. La malattia scompare in una settimana, ma se le vie biliari sono infette, le ricadute sono possibili per molti anni. Le cisti si combattono iodando l'acqua.
Scoperto dallo scienziato ceco Vilém Lambl nel 1859Giardia lamblia. Da allora, il più semplice ha cambiato diversi nomi, e quello attuale è stato dato in onore dell'esploratore e parassitologo francese Alfred Giar, che non ha descritto Lamblia.
E il primo schizzo di Giardia fu fatto da Anthony van Leeuwenhoek, che lo trovò sulla sua sedia arrabbiata. Era il 1681.
Giardia è anche molto vecchia dal punto di vista evolutivo, proviene quasi direttamente dall'antenato di tutti gli eucarioti.
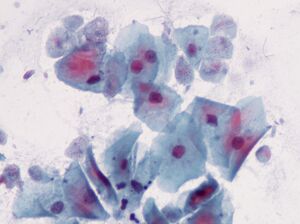
Il più intimo. Trichomonas vaginalisTrichomonas vaginalis.
Il più semplice che viene trasmesso sessualmente. Vive nella vagina e negli uomini - si trasmette sessualmente o attraverso salviette umide nell'uretra, nell'epididimo e nella prostata. I bambini possono essere infettati attraverso il canale del parto.T. vaginalisha 4 flagelli all'estremità anteriore e una membrana ondulata relativamente corta che rilascia pseudopodi quando necessario. La dimensione massima di Trichomonas è di 32 x 12 micron.
Trichomonas èpiù comunedegli agenti eziologici di clamidia, gonorrea e sifilide combinati. Colpisce circa il 10% delle donne e forse più dell'1% degli uomini. Quest'ultimo numero è inaffidabile perché è più difficile individuare il parassita negli uomini.
T. vaginalissi nutre di microrganismi, inclusi i batteri lattici della microflora vaginale, che mantengono un ambiente acido, creando un pH ottimale per se stesso superiore a 4. 9.
Il Trichomonas distrugge le cellule della mucosa e provoca infiammazione. Circa il 15% delle donne infette lamenta sintomi.
Viene trattatocon un farmaco antibatterico. Si consiglia di fare una doccia regolare con aceto diluito come misura preventiva.
Descritto nel 1836 dal batteriologo francese Alfred Donne. Lo scienziato non ha capito che c'era un parassita patogeno di fronte a lui, ma ha determinato le dimensioni, l'aspetto e il tipo di movimento del più semplice.
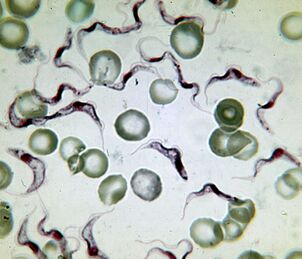
Il più letale. L'agente eziologico della malattia del sonnoTrypanosoma brucei
L'agente eziologico della malattia del sonno africana è il protozoo più letale. Una persona infetta muore senza cure. Il tripanosoma è un flagellato allungato di 15-40 µm di lunghezza. Esistono due sottospecie che non possono essere distinte esternamente. Malattia causata daT. brucei gambiense, dura 2-4 anni.T. brucei rhodesienseè un patogeno temporaneo più virulento dal quale muoiono dopo pochi mesi o settimane.
Distribuitoin Africa tra il 15 ° parallelo dell'emisfero meridionale e settentrionale nell'area naturale del vettore - insetti succhiatori di sangue del genereGlossina(mosca tsetse). Delle 31 specie di mosche, 11 sono pericolose per l'uomo. La malattia del sonno colpisce la popolazione di 37 paesi a sud del Sahara a 9 milioni di km di distanza2. Fino a 20. 000 persone si ammalano ogni anno. Adesso ci sono circa 500. 000 pazienti, 60 milioni sono a rischio.
Dall'intestino delle moscheT. bruceientra nel flusso sanguigno umano, da lì nel liquido cerebrospinale e influenza il sistema nervoso. La malattia inizia con febbre e infiammazione delle ghiandole linfatiche, seguite da letargia, sonnolenza, paralisi muscolare, esaurimento e coma irreversibile.
La letalità del parassita è correlata alla sua capacità di attraversare la barriera emato-encefalica. I meccanismi molecolari non sono completamente compresi, ma è noto che il parassita secerne proteasi di cisteina quando entra nel cervello e utilizza anche alcune proteine ospiti. Nel sistema nervoso centrale, invece, il tripanosoma protegge dai fattori immunitari.
La prima descrizione della malattia del sonno nella parte alta del Niger fu lasciata dallo studioso arabo Ibn Khaldun (1332-1406). Già all'inizio del XIX secolo, gli europei erano a conoscenza dei primi segni della malattia: gonfiore dei linfonodi del collo (un sintomo di Winterbottom) e i commercianti di schiavi gli prestavano particolare attenzione.
ScopertoT. bruceiIl microbiologo scozzese David Bruce, da cui prende il nome, stabilì per primo la connessione tra il tripanosoma, la mosca tse-tse e la malattia del sonno nel 1903.
Il trattamentodipende dallo stadio della malattia e i farmaci provocano gravi effetti collaterali. Il parassita ha un'elevata variabilità antigenica, rendendo impossibile la produzione di un vaccino.
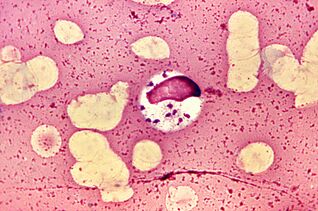
Il più stravagante. LeishmaniaLeishmania donovani
Leishmania si sono guadagnate il titolo di parassiti più stravaganti perché vivono e si moltiplicano nei macrofagi, cellule progettate per distruggere i parassiti.L. donovaniè il più pericoloso di loro. Provoca leishmaniosi viscerale, febbre colloquiale di dumdum o kala azar, da cui quasi tutti i pazienti muoiono senza trattamento. Ma i sopravvissuti acquisiscono l'immunità a lungo termine.
Esistono tre sottospecie del parassita.L. donovani infantum(Mediterraneo e Asia centrale) colpisce principalmente i bambini, i cani sono spesso il suo serbatoio.L. donovani donovani(India e Bangladesh) è pericoloso per adulti e anziani e non ha riserve naturali. L'americanoL. donovani chagasi(America centrale e meridionale) può vivere nel sangue dei cani.
L. donovani- Flagellato non più lungo di 6 micrometri. Le persone vengono infettate dopo essere state morse da zanzare del generePhlebotomus, a volte attraverso il contatto sessuale, i bambini - che passano attraverso il canale del parto. Nel sangue,L. donovanipenetra nei macrofagi che trasportano il parassita attraverso gli organi interni. Il parassita si moltiplica nei macrofagi e li distrugge. Il meccanismo di sopravvivenza molecolare nei macrofagi è piuttosto complesso.
Sintomi della malattia- febbre, ingrossamento del fegato e della milza, anemia e leucopenia, che contribuiscono all'infezione batterica secondaria. Ogni anno 500. 000 persone sviluppano la leishmaniosi viscerale e circa 40. 000 muoiono.
Trattamentopesante: antimonio per via endovenosa e trasfusione di sangue.
Affiliazione tassonomicaL. donovaniè stata definita nel 1903 dal famoso ricercatore sulla malaria e vincitore del Premio Nobel Ronald Ross. Deve il suo nome generico a William Leishman e il nome specifico a Charles Donovan, che nel 1903 scoprì autonomamente cellule protozoiche nella milza dei pazienti morti di Kala Azar, uno a Londra, l'altro a Madras.
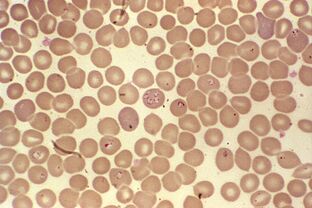
Il ciclo di vita più difficile.Babesia spp.
La babesia, oltre alla riproduzione asessuata in più fasi negli eritrociti dei mammiferi e negli acari sessuali nell'intestino del genereIxodes, ha reso più difficile il loro sviluppo attraverso la trasmissione transovariale. Gli sporozoiti protozoi penetrano nelle ovaie dall'intestino di un acaro femmina e infettano gli embrioni. Quando le larve degli acari si schiudono, i babesia invadono le loro ghiandole salivari ed entrano nel sangue del vertebrato al primo morso.
DistribuitoBabesia in America, Europa e Asia. I loro serbatoi naturali sono roditori, cani e bovini. Una persona è infettata da diversi tipi: B. microti, B. divergens, B. duncanieB. venatorum.
I sintomi della babesiosi sono simili alla malaria: febbre ricorrente, anemia emolitica, ingrossamento della milza e del fegato. La maggior parte delle persone guarisce spontaneamente, ma la babesiosi è fatale in quelli con un sistema immunitario compromesso.
Metodi di trattamentosono ancora in fase di sviluppo mentre vengono prescritti antibiotici e, nei casi più gravi, trasfusioni di sangue.
Babesia fu descritta dal microbiologo rumeno Victor Babes (1888), che la scoprì in mucche e pecore malate. Decise che si trattava di un batterio patogeno, che chiamòHaematococcus bovis. La babesia è stata a lungo considerata un patogeno animale fino a quando non fu scoperta nel 1957 in un pastore jugoslavo morto per un'infezione da B. divergens.
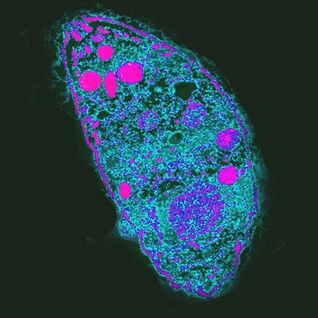
Il più influente. L'agente eziologico della toxoplasmosiToxoplasma gondii
T. gondiiè il parassita più potente perché controlla il comportamento degli host intermedi.
Distribuito ovunque, distribuito in modo non uniforme. Ad esempio, in Francia l'84% della popolazione è infetta e nel Regno Unito il 22%.
Il ciclo di vita del Toxoplasma consiste di due fasi: asessualmente, nel corpo si verifica qualsiasi riproduzione sessuale a sangue caldo, che è possibile solo nelle cellule epiteliali dell'intestino del gatto. PerT. gondiipotrebbe completare lo sviluppo, il gatto deve mangiare un roditore infetto. Rendendo più probabile questo evento,T. gondiiblocca la naturale paura dei roditori per l'odore dell'urina di gatto e lo rende attraente prendendo di mira un gruppo di neuroni nell'amigdala. Come lo fa è sconosciuto. Uno dei sospetti meccanismi d'azione è una risposta immunitaria locale a un'infezione. Cambia i livelli di citochine, che a sua volta aumenta i livelli di neuromodulatori come la dopamina. Il toxoplasma influisce anche sul comportamento umano, che si manifesta anche a livello di popolazione. Nei paesi con alti livelli di toxoplasmosi, il nevroticismo e il desiderio di evitare nuove situazioni pericolose sono più comuni. È possibile che l'infezione daT. gondiipossa portare a cambiamenti culturali.
L'infezionenegli esseri umani è spesso asintomatica, ma se l'immunità è indebolita, distrugge le cellule del fegato, dei polmoni, del cervello e della retina e provoca la toxoplasmosi acuta o cronica. Il decorso dell'infezione dipende dalla virulenza del ceppo, dallo stato del sistema immunitario dell'ospite e dalla sua età - gli anziani sono meno sensibili a questoT. gondii.
Trattala toxoplasmosi con farmaci antiprotozoari.
Descrittonel 1908 sui roditori del deserto. Questo premio appartiene al personale dell'Istituto Pasteur in Tunisia, Charles Nicolas e Luis Manso.
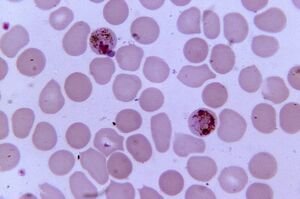
Più patogeno. Plasmodium malariaPlasmodium spp.
La malaria da Plasmodium è il parassita più patogeno nell'uomo. Il numero di malati di malaria può raggiungere i 300-500 milioni, il tasso di morte per epidemie 2 milioni. La malattia provoca ancora tre volte più vite rispetto ai conflitti armati.
Cinque tipi di Plasmodium causano la malaria negli esseri umani:Plasmodium vivax, P. falciparum, P. malariae, P. ovaleeP. knowlesi, che colpiscono anche i macachi.
Distribuitonell'area dei vettori - zanzareAnopheles, che richiedono una temperatura di 16–34 ° C e un'umidità relativa superiore al 60%.
Un confronto del genoma del plasmodia più virulento,P. falciparum, con il gorilla plasmodia suggerisce che gli umani dei loro antenati siano stati infettati da queste scimmie. L'emergere di questa forma di Plasmodium è legata all'emergere dell'agricoltura in Africa, che ha portato ad un aumento della densità di popolazione e allo sviluppo dei sistemi di irrigazione.
I plasmodi si riproducono sessualmente nell'intestino delle zanzare e nel corpo umano è un parassita intracellulare che vive negli epatociti e negli eritrociti e si riproduce fino allo scoppio delle cellule. 1 ml di sangue del paziente contiene da 1 a 50. 000 parassiti.
La malattia si manifesta con infiammazione, febbre ricorrente e anemia. In caso di gravidanza, è pericoloso sia per la madre che per il feto. I globuli rossi infettati conP. falciparumostruiscono i capillari e nei casi più gravi si sviluppa ischemia degli organi interni e dei tessuti.
Il trattamentorichiede una combinazione di diversi farmaci e dipende dallo specifico patogeno. I plasmodi diventano resistenti ai farmaci.








































